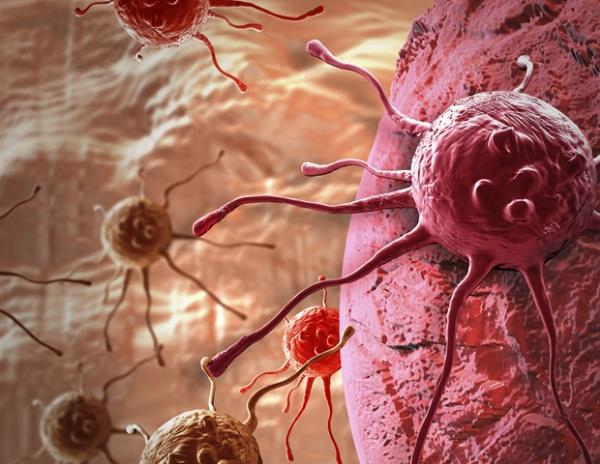
在马萨诸塞州斯普林菲尔德贝斯特医疗中心的先锋谷生命科学研究所(PVLSI)进行的实验。该研究证实,马萨诸塞大学阿默斯特分校化学工程师尼尔·福布斯的传递和触发系统首次成功地将TRAIL(一种抗癌蛋白)直接植入实体肿瘤中,并适时地将其激活。这种治疗将患有乳腺肿瘤的小鼠的30天存活率从0提高到100%。
“这是第一步,但这是我们第一次控制向肿瘤的输送,也是我们第一次能够启动细胞毒性蛋白的产生,并从内部杀死肿瘤。通过更多的工作,我们应该能够调整我们的方法,”福布斯说。“作为一名工程师,我设计的是运输和部署,也就是说,一种让军队就位的方式,加上一个开关,向那些部队发出武装和攻击的信号。”
福布斯说,大约10年前,人们就知道沙门氏菌和埃希氏菌等常见细菌有利于实体肿瘤的微环境。当其他人设计出一种非致病性沙门氏菌菌株时,福布斯看到了机会。他开始设计一种“部队运输”,这种运输在地点和时间上都是可控的,在攻击肿瘤细胞的同时对病人的伤害更小。
福布斯设计的实验由PVLSI外科肿瘤学家Sabha Ganai进行,她因此获得了博士学位。他们报告说,他们成功地将数百万种鼠伤寒沙门氏菌(S. typhimurium)注入小鼠乳腺肿瘤,并触发它们开始产生肿瘤坏死因子相关的凋亡诱导配体(TRAIL),这是一种对癌细胞有毒的肽。它选择性地导致肿瘤细胞死亡或凋亡,而宿主毒性最小,即不损害正常细胞。
他们首先对沙门氏菌进行改造,使其包含TRAIL基因,从而使其在RecA启动子的控制下表达。然后,Ganai将200万个携带工程RecA启动子和TRAIL基因的鼠伤寒沙门氏菌细胞注射到具有乳腺肿瘤(即乳腺癌)的基因相同的小鼠组中。当细胞受到任何原因的DNA损伤时,RecA启动子就会激活。在这种情况下,Ganai和Forbes使用非常低剂量的2 Grey伽马射线来启动RecA。
注射后约48小时,每个肿瘤的细菌数量增加到约1000万个。在这一点上,Ganai将小鼠暴露于单剂量或两次低剂量辐射中的第一次。由此产生的对DNA的轻微损伤(单链断裂)激活了RecA,并启动了TRAIL的工程生产,TRAIL对癌细胞具有高度毒性。
接受两次低剂量放射治疗并注射细菌以触发RecA启动子的小鼠,肿瘤体积减少,存活时间比对照组更长。福布斯说,TRAIL清除得很快,为了达到最佳效果,必须定期重新刺激其释放。因此,双剂量放疗组表现最好。
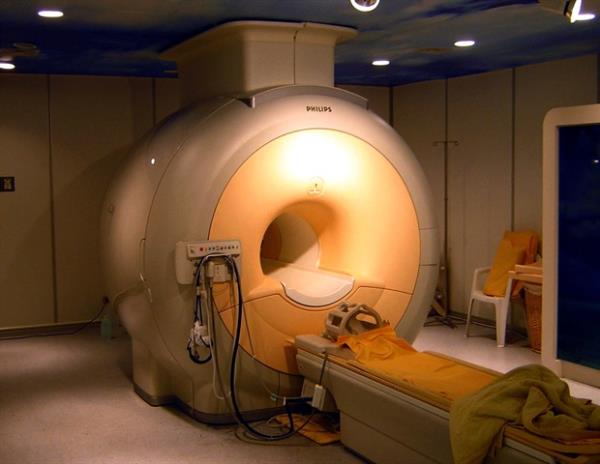
Forbes和Ganai说,这些实验表明,他们可以通过改造鼠伤寒沙门氏菌的基因开关来控制细菌产生抗肿瘤药物的时间,这种基因开关可以对辐射做出反应。这意味着细菌可以给未来的病人,一旦细菌在肿瘤中定植,肿瘤临床医生就可以照射肿瘤,让细菌开始制造药物。辐射是一个很好的转变,因为它可以穿透人体组织,在大多数癌症中心都可以使用,而且低剂量是无害的。
Ganai和Forbes设想,一旦完全开发,“这种具有空间和时间控制的细菌癌症治疗将通过提高疗效同时限制宿主毒性来提供可观的治疗效益。”