在最近发表在《神经病理学学报》上的一项研究中,研究人员利用全基因组测序(WGS)和途径分析发现了APOEε4携带者抗阿尔茨海默病(AD)的保护性遗传变异。
背景
阿尔茨海默病的特点是进行性记忆丧失和认知能力下降,通常在很长一段时间内没有症状。尸检时,AD大脑通常显示β-淀粉样斑块和tau蛋白的神经原纤维缠结。尽管对阿尔茨海默病的理解有了进步,但阿尔茨海默病在很大程度上仍然无法治愈,现有药物提供的缓解作用微乎其微,这主要是由于对其病理机制的了解不完全。遗传因素,尤其是APOEε4等位基因,在个体和种族群体中显著影响疾病的变异性。这种等位基因的影响各不相同,一些携带者的症状较轻或较晚,这表明需要进一步研究来解释这些复杂的基因相互作用,并开发更好的治疗和诊断方法。
一个关于这项研究
研究中的所有人类样本都被去识别,以确保研究人员无法从捐赠者那里推断或获取个人信息。在生成临床数据之前,获得了哥伦比亚大学欧文医学中心和梅奥诊所机构审查委员会的批准。该研究还包括动物实验,实验遵循哥伦比亚大学机构动物护理和使用委员会(IACUC)在ACAABN3554批准协议下的指导方针。该计划遵循AAALAC国际认可的标准,并与公共卫生服务机构保持动物福利保证。
在斑马鱼研究中,使用了野生型AB菌株和fn1b−/−纯合敲除鱼种,年龄从8至10个月,雌雄同体。为了确保一致性,实验动物从同一窝随机分配到不同的实验条件。
本研究的人类队列包括基于NIA-AD家族的研究(NIA-AD FBS),该研究涉及美国的多个家族。家庭的选择是基于至少有一个成员在60岁以后被诊断为明确或可能的阿尔茨海默病,并且有一个兄弟姐妹有类似的发病。这些参与者有详细的人口统计和临床数据。华盛顿高地/因伍德哥伦比亚老年化项目从曼哈顿北部招募了65岁及以上的人来研究痴呆症的临床和遗传风险因素。阿尔茨海默病遗传研究中心(EFIGA)针对不同的种族群体,包括来自波多黎各、多米尼加共和国和纽约的家庭,以确定APOEε4健康携带者的保护性等位基因。
所有程序,从动物的照顾和使用到样品的处理,都是在相关当局批准的道德标准和协议下进行的,确保了高度的科学诚信和对参与研究的人类和动物受试者的尊重。
研究结果
本研究访问了来自700多个非西班牙裔白人和加勒比西班牙裔家庭的3578名个体的WGS数据,这些家庭都受到AD的影响。通过对WGS数据的统一和质量控制,研究人员在认知能力不受影响的老年APOEε4携带者中发现了罕见的编码变异。这些携带者,无论是纯合的还是杂合的,都具有非携带者所没有的罕见变异。这项研究优先考虑了可能对蛋白质产物有害的变异,在476个基因中发现了510个变异,特别是在纤维连接蛋白1 (FN1)基因中。
基因本体分析进一步揭示了在鉴定的变异中细胞外基质(ECM)相关过程的强烈富集。这表明ECM成分的功能改变可能为APOEε4携带者提供保护机制,表明APOEε4相关的ECM成分的增加可能被这些基因的功能缺失变体所抵消。两个重要的基因,胶原型VI α - 2链(COL6A2)和FN1,检测了可能通过带电残基的变化影响ECM稳定性的变异,假设影响蛋白质功能。
进一步的分析涉及来自阿尔茨海默病遗传联盟(ADGC)和英国生物银行(UKB)等数据库的独立队列,重点关注非西班牙裔白人个体,以测试研究结果的重复性。FN1的变异rs140926439在APOEε4纯合携带者中显示AD的风险显著降低,证实了该变异对AD的保护作用。此外,敏感性分析证实了这些发现,强化了该变异作为AD进展保护因素的潜力。
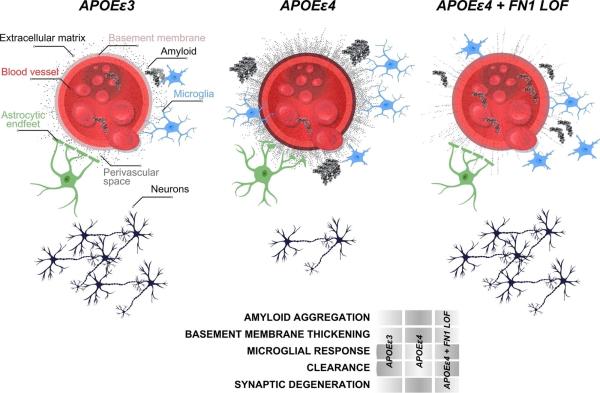
本研究还探讨了APOEε4剂量与血脑屏障中FN1沉积的相关性。不同APOE基因型个体脑组织的免疫染色分析显示,随着APOEε4剂量的增加,FN1水平升高,纯合子携带者尤其明显。
最后,利用斑马鱼模型研究了FN1在调节淀粉样蛋白毒性反应中的潜在作用。在斑马鱼中,FN1功能的丧失导致淀粉样蛋白治疗后胶质血管相互作用减少和胶质反应减少,这表明纤维连接蛋白可能在淀粉样蛋白清除的调节中发挥关键作用。这与FN功能丧失变异可能通过增强有毒蛋白聚集体的清除和调节免疫系统活性来预防AD病理的假设一致。