最近发表在《自然》杂志上的一项研究展示了大鼠耐力训练的时间效应的全生物体分子图谱。
背景
经常锻炼有很多好处,比如降低患癌症、神经系统和心脏代谢疾病的风险,以及降低全因死亡率。运动几乎影响所有的器官系统,由于组织和器官系统之间和内部的分子/细胞适应,运动产生了有益的影响。
一些组学平台(组学),如表观基因组学、转录组学、代谢组学和蛋白质组学,已经被用来研究这些事件。
然而,研究往往集中在覆盖一个或两个基因组的单个组织上,并且存在偏见。需要一个全面的、全机体的、多组学的运动效果图。
为此,已经建立了身体活动分子传感器联盟,以建立动物不同组织以及人类血液、脂肪组织和骨骼肌对运动反应的分子图谱。
研究结果
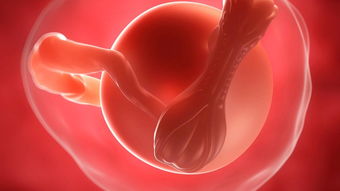
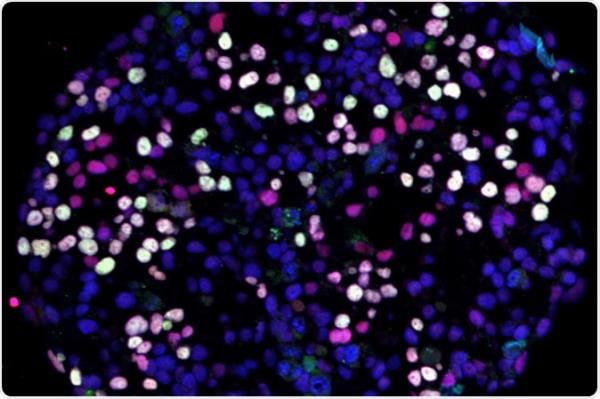
本研究展示了大鼠耐力训练效应/反应的全生物分子图谱。首先,344只大鼠进行1周、2周、4周或8周的渐进式跑步机运动(耐力训练)。最后一次训练后48小时采集组织。性别匹配、未经训练、久坐不动的老鼠作为对照组。
训练导致了强大的表型变化,在8周时,雌性和雄性大鼠的有氧能力分别增加了16%和18%。
八周后,男性的体脂减少了5%,瘦质量没有明显变化。在4周或8周的训练后,女性的体脂率没有变化。
使用多组学技术分析全血、18种实体组织和血浆。分子分析优先考虑生物学相关性和(可用的)组织数量。
总体而言,在211个组织组合和分子平台上进行了9466次分析,导致超过60万次非表观遗传和1430万次表观遗传测量。
在所有基因组的大多数组织中都观察到训练调节分子。对于转录组学,腔静脉、睾丸、皮质和下丘脑具有最少的训练调节基因,而血液、结肠、肾上腺和脂肪组织具有广泛的影响。
对于蛋白质组学,心脏、肝脏和腓肠肌在蛋白质丰度和翻译后修饰方面具有显著的差异调节。
对于代谢组学,所有组织一致表现出最大的代谢物差异。接下来,选择具有广泛分子谱的6个组织(肾、肺、白色脂肪组织、腓肠肌、心脏和肝脏)来评估训练反应性基因表达。
总体而言,7115个独特基因绘制了11407个差异特征。大约67%具有≥一个训练反应特征的基因是组织特异性的。
此外,2359个基因在至少两个组织中具有差异特征,白色脂肪组织和肺部独特地共享最大的基因集,主要是免疫相关的。所有6个组织共有22个训练调节基因,特别是在热休克反应途径中富集。
造血相关转录因子在血液中富集,而肌细胞增强因子2 (Mef2)家族转录因子基序在骨骼肌和心脏中富集。
几个显著激酶的磷酸化特征在几个组织中被改变。接下来,将差异特征与完整的时间统计汇总聚类,以比较跨组织训练的多组学反应。对几个簇进行了途径富集分析,并检查了与训练相关的生物过程。
与其他组织相比,肝脏具有实质性的染色质可及性调节。血液中含有与细胞器生物发生/维持和翻译有关的富集物。
在腓肠肌中,与脂质合成/降解和过氧化物酶体增殖物激活受体(PPAR)信号相关的术语在蛋白质水平上富集。与此相反,与甘油磷脂代谢和醚脂代谢相关的蛋白在代谢组学水平上富集。
值得注意的是,血浆和小肠在1周和2周的训练中有更多的变化。此外,在许多组织中观察到对训练反应的性别差异,58%的训练调节特征在8周时发生性别分化。
在肺磷酸基、肝乙酰基、肾上腺和白色脂肪组织转录本中,两性之间的反应相反。促炎细胞因子在一些组织中表现出性别差异。
大多数女性特异性细胞因子在训练的第1周和第2周之间表现出不同的调节。相反,在训练的第4周和第8周之间观察到大多数男性特异性细胞因子的差异调节。
此外,肾上腺表现出广泛的转录重塑,有超过4000个差异调节基因。在肺部,雄性的磷信号活性随着训练而下降。
最后,总结了整个生物体的代谢变化。肝脏、心脏、肺和海马体的代谢物种类最丰富。
对酰基肉碱群和个体代谢物的进一步研究揭示了与训练反应的功能改变有关的变化。肾脏中的皮质醇水平显著升高。
肝脏中的代谢途径在脂质组、蛋白质组和乙酰组中受到实质性的调节,其中12类脂质和脂质相关化合物的代谢物显著富集。
大多数肝脏特征与氨基酸、线粒体和脂质代谢途径的变化相对应。磷脂酰胆碱升高,同时甘油三酯降低。
结论
本研究采用25个多组织分子平台,报道了大鼠耐力训练反应的时间动态。在mRNA转录物、蛋白质和代谢物的组织中观察到数千种训练反应性变化。
许多变化与人类健康有关,包括心血管健康和组织损伤/恢复。总的来说,这些发现有助于理解运动对健康和疾病的改善。